Detekce bodových a delečních mutací genu egfr1 a genu k-ras u pacientů s karcinomem plic
Plicní nádory zaujímají v celosvětovém měřítku druhé místo mezi všemi maligními onemocněními. V České republice jsou na prvním místě v příčinách úmrtí na zhoubné nádory. Nejčastější incidence nádorů plic je ve věku 55 až 80 let, při čemž většina nádorů (až 80% nově odhalených případů rakoviny plic) je diagnostikována v pokročilém stádiu onemocní.
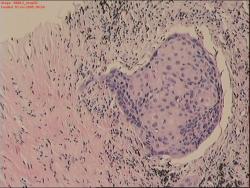
Nemalobuněčný plicní karcinom (NSCLC), (parafinový řez, hematoxylin-eosin).
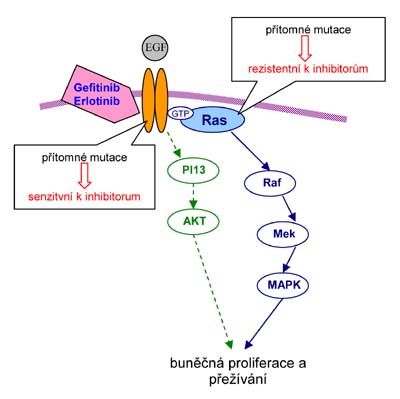
Standardní terapie nemalobuněčných karcinomů využívá běžných cytostatik. Tato léčba však nezaznamenává dobrých výsledků, proto je snaha o vývoj jiných druhů protinádorové léčby, především biologické povahy. Studium biologických procesů v nádorových buňkách ukázalo, že k maligní transformaci značnou měrou přispívají nekontrolované aktivace membránových receptorů. Tento fakt vede k tomu, že nádorová buňka je nezávislá na růstových faktorech a vymyká se tak přísnému řízení proliferace v mnohobuněčném organismu. U buněk řady solidních nádorů epiteliálního původu taková aktivace byla popsána u receptoru pro epidermální růstový faktor (EGFR1, ErbB/HER).
Ke zvýšené aktivaci Egfr1 dochází overexpresí genu egfr1, která je způsobena amplifikací genu v genomu nádorové buňky. Rovněž aktivující jsou mutace tyrozinkinázové domény receptoru (exon 18 – 21), které zapříčiňují spuštění signální transdukce bez vazby ligandu k vazebné doméně receptoru.
Proti aktivovanému Egfr1 je zaměřena cílená terapie nízkomolekulárními inhibitory tyrozinkináz. Od roku 2004 byl v České republice v klinickém testování preparát nízkomolekulárních inhibitorů u pacientů s nemalobuněčným plicním karcinomem IRESSA (gefitinib, ZD1839, 4-quinazolinamin) a od roku 2005 je používán preparát TARCEVA (erlotinib, OSI-774).
Podání těchto léčiv by mělo předcházet vyšetření amplifikace genu egfr1 v souvislosti s jeho overexpresí případně detekce přítomných mutací v tyrozinkinázové doméně egfr1.
Naše pracoviště má zavedené metody na vyšetření genu egfr1 na všech úrovních.
Značný počet pacientů s bronchoalveolárním karcinomem na léčbu nízkomolekulárními inhibitory nevykazuje požadovanou odpověď. Bylo zjištěno, že u zhruba u 30-40% rezistentních pacientů jsou přítomné mutace onkogenu k-ras. U genu K-ras jsou nejběžněji přítomné bodové mutace kodónu 12 v 1. exonu (především je detekovaná záměna glycinu za valin, či asparagin). Často se také objevují bodové mutace kodónu 13 a méně často kodónu 61. Všechny popisované mutace jsou aktivující a vedou k narušení intracelularní signalizace podobně jako v případě aberantní aktivace proteinu Egfr1.
Na velkých klinických studiích bylo prokázáno, že mutace genu k-ras jsou běžné především u kuřáků a téměř se nevyskytují u pacientů s popsanou mutací v genu egfr1. Stejně tak je dnes zřejmé, že u pacientů s detekovanou mutací v genu k-ras je možné předpokládat 100% rezistenci k léčbě nízkomolekulárními inhibitory Egfr1. Proto by bylo vhodné provést i toto vyšetření před nasazením nákladné terapie TARCEVOU.